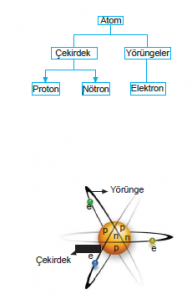
Atom Yapısı
Çekirdek
Proton ve nötron taneciklerini kapsar. Atomun kütlesini çekirdek oluşturur. Atomun en yoğun bölgesidir.
Proton
Atomun çekirdeğinde bulunan (+) yüklü taneciklerdir. Sembolü “p” dir.
Proton sayısı = Atom numarası = Çekirdek yükü
- Her elementin proton sayısı farklıdır.
Nötron
Atomun çekirdeğinde bulunan yüksüz (nötr) taneciklerdir. Sembolü “n” dir.
Elektron
Atomun yörüngelerinde yer alan yani çekirdeğin etrafın- da dönen hareketli taneciklerdir. (–) yüklüdür. Sembolü “e” dir.
Kütle Numarası
Atomun kütlesi çekirdeğinde toplanmıştır. Bu nedenle çekirdeğindeki taneciklerin toplam kütlesi, kütle numara- sını verir.
Kütle numarası = Proton + Nötron
Kütle numarası, nükleon sayısı olarak da bilinir.
Nötr Atom
Atomun proton sayısının elektron sayısına eşit olduğu durumdur.
Atomun yüksüz halidir.
Nötr bir atomda,
Proton sayısı = Elektron sayısıdır.
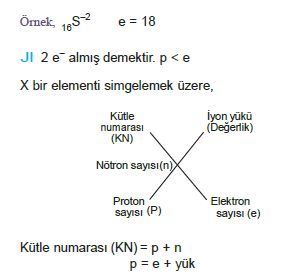
Örnek, 11Na İyon
p = 11 e = 11
Atomun elektron almış veya elektron vermiş halidir.
a. Katyon
Nötr bir atom elektron verirse (+) yüklü hale geçer. Bu iyona “katyon” denir.
Örnek, 11Na
e = 10
- 1e vermiş demektir. p > e
b. Anyon
Nötr bir atom elektron alırsa (–) yüklü hale geçer. Bu iyo na “anyon” denir.
ÖRNEK:Pozitif yüklü iyonlarla ilgili,
I. Proton sayısı elektron sayısından fazladır.
II. Nötron sayısı elektron sayısından azdır.
III. Çekirdek yükü elektron sayısına eşittir.
yargılarından hangileri kesinlikle doğrudur?
A) Yalnız I B) I ve II C) I ve III D) II ve III E) I, II ve III
ÇÖZÜM: Pozitif yüklü iyon katyondur. Katyonlarda p > e ilişkisi vardır. Nötron sayısı büyük, küçük ya da eşit olabilir. Çe- kirdek yükü proton sayısıdır.
YANIT:A
ÖRNEK: X atomu Y–3 iyonuna 2 elektron verirse, son durum- da X ve Y taneciklerinin yükü kaç olur?
A) 0, –5 B) – 2, –1 C) – 2, –3 D) +2, –1 E) +2, –5
ÇÖZÜM: Elektron alan tanecik aldığı elektron kadar (–) yükle yük- lenir. Elektron veren ise (+) yükle yüklenir.
Yanıt E
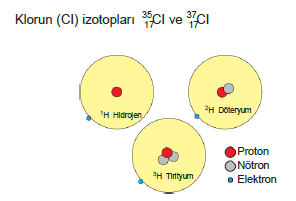
İzotop Atomlar
Proton sayıları, aynı nötron sayıları farklı olan atomlardır. Bu atomların nötron sayıları farklı olduğundan kütle numaralarıda farklı olur.
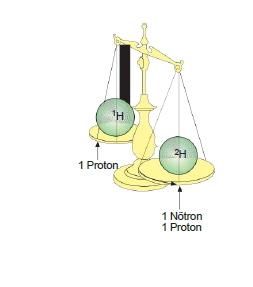
- Bir elementin izotop nötr atomlarının kimyasal özel- likleri aynıdır. Fiziksel özellikleri ise farklıdır.
- İzotop olan fakat elektron sayıları farklı olan tanecik- lerin ise fiziksel ve kimyasal özellikleri farklıdır.
ÖRNEK: Bir elementin atom numaraları aynı, kütle numaraları farklı çeşitlerine o elementin izotopları denir. Birbirinin izotopu olan iki nötr atomun yapısı ile ilgili,
I. Proton sayıları farklı, elektron sayıları aynıdır.
II. Proton ve nötron sayıları farklıdır.
III. Nötron sayıları farklı, elektron sayıları aynıdır.
açıklamalarından hangileri doğrudur?
A) Yalnız I B) Yalnız II C) Yalnız III D) I ve II E) I ve III
1992 ÖYS
ÇÖZÜM: İzotop atomların proton sayıları aynı, nötron sayıları fark- lıdır. Nötr bir atomun proton sayısı aynı zamanda elekt- ron sayısına eşittir.
Yanıt C
İzoton Atomlar
Proton sayıları farklı, nötron sayıları aynı olan ele- mentlerdir. Bu atomların hem kimyasal, hem de fiziksel özellikleri farklıdır.
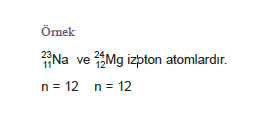
İzobar Atomlar
Proton sayıları farklı, kütle numaraları (nükleon sayıları) aynı olan elementlerdir. Bu atomların hem kimyasal hem de fiziksel özellikleri farklıdır.

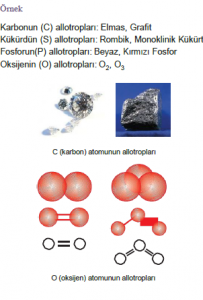
Allotrop Atomlar
Bir elementin özdeş atomlarının farklı sayı ve dizilişteki şekilleridir. Bu atomlar aynı elemente ait olduğu için kim- yasal özellikleri aynıdır. Atomlar farklı sayı ve dizilişte olduğundan fiziksel özellikleri farklı olur.
ÖRNEK: Bir elementin aynı cins atomlarının farklı kristal veya molekül şekillerinin her birine, o elementin allotropu denir. Bu tanıma göre, aşağıdakilerin hangisinde verilen maddeler birbirinin allotropu değildir?
A) Oksijen – Ozon
B) Grafit – Elmas
C) Kırmızı fosfor – Beyaz fosfor
D) Radyoaktif iyot – Radyoaktif olmayan iyot
E) Rombik kükürt – Monoklinik kükürt
1992 ÖYS
ÇÖZÜM 😀 seçeneğinde iyot hakkında verilen özellik radyoaktivi- teyle ilgilidir. Aynı olan atomların çekirdeğindeki nötron sayılarının farklı oluşu bu özelliği belirler. Proton sayıları aynı, nötron sayıları farklı bu atomlar birbirinin izotopu- dur.
Yanıt D
[kimya_ygs_lys]