Kimyasal Bağlar
Atomları veya atom gruplarını birarada tutmaya yarayan kuvvete kimyasal bağ denir.
Atomlar bağ oluşturduklarında kararlı yapıya ulaşır. Bu kararlılık, atomun son yörüngesindeki elektron sayısını sekize tamamlamasıyla gerçekleşir. Bu kurala okted kuralı denir.Atomun değerlik elektron sayısını ikiye tamamlamasına ise dublet kural denir.
Dublet kuralına göre bağ yapan atomlar elektron düzenini 2He soygazına benzetir.
Kimyasal bağlar ikiye ayrılır iyonik ve kovalent bağlar.
1. İyonik Bağlar
Bir metal atomu ile bir ametal atomu arasında kurulan bağdır. Metaller kararlı yapıya ulaşmak için (soygazabenzemek) elektron verirler ve bu nedenle (+) yükle yüklenirler. Ametaller ise kararlı yapıya ulaşmak için elektron alırlar ve (–) yükle yüklenirler. (+) yüklü metal iyonu ile (–) yüklü ametal iyonu arasında elektron alış verişine dayalı olarak bir elektrostatik çekim kuvveti oluşur. Bu çekim kuvveti sonucu oluşan iyonik bağ oldukça kuvvetlidir.

NOT: İyonik karakteri en yüksek bağ, en aktif metal ile en aktif ametal arasında oluşur.
En aktif metal Æ 7 periyot
1A grubu metalı (Fr) En aktif ametal Æ 2 periyot
7A grubu ametali (F)
2. Kovalent Bağlar
Ametal atomları arasında oluşan bağlardır. Bu bağda elektron paylaşımı (ortaklaşması) gerçekleşir. Kovalent bağlar ikiye ayrılır.
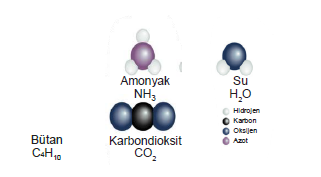
a. Polar (Kutuplu) Kovalent Bağlar
Farklı ametaller arasında oluşan bağlardır. Bu bağda elektronegatifliği büyük olan ametal atomu, elektronları kendi üzerine daha fazla çekeceğinden kısmi olarak (– ) yükle yüklenir. Diğer ametal atomu ise kısmi olarak (+) yükle yüklenir. Yani molekülde (+) ve (–) yüklü bir kutup- laşma meydana gelir. Bu elektronegatiflik farkı (elektron çekme yeteneği) ne kadar büyükse bağ da o kadar polar olur.

b. Apolar (Kutupsuz) Kovalent Bağlar
Aynı ametal atomları arasında oluşan bağa denir. Bu bağda elektronlar aynı ametaller (eşit kuvvette) tarafın- dan çekileceğinden molekülde kutuplaşma olmaz.

İyonik Bağlı Bileşiklerin Özellikleri
1. Kristal yapılıdırlar.
2. Sulu çözeltileri ve sıvı halleri iyon hareketi ile elektrik akımını iletir.
NOT:İyonik bileşiklerin katı halde elektriği iletememesinin nedeni, iyonların birbirine sıkı sıkı bağlı olması ve bu sebeple de hareket edememesidir.
3. En kuvvetli bağa sahip iyonik bileşikler, iyonlaşma enerjisi en düşük metal (elektronu kolaylıkla veren) ile elektronegatifliği en yüksek ametal (elektronu en kolay çeken) arasında oluşur.
4. Oda koşullarında (25 °C, 1 atm) katı halde bulunur- lar.
5. Erime ve kaynama noktaları yüksektir.

[kimya_ygs_lys]
