Redoks Tepkimelerinin Denkleştirilmesi
Redoks tepkimelerinde atomların türleri, sayıları ve elektrik yüklerinin eşit olması gerekir.
Redoks tepkimeleri iki yöntemle denkleştirilir.
I. Değerlik yöntemi
II. Yarı tepkime (iyon – elektron) yöntemi
1. Değerlik Yöntemi
- Atomların değerlikleri bulunur ve değerliği değişen atomlar belirlenir.
- İndirgenme ve yükseltgenme sonucu alınan ve veri-len elektronları eşitlemek amacıyla indirgenen ve yükseltgenen atomların başına gerekli katsayılar ya-zılır.
- Atom türleri ve sayılarını eşitlemek amacıyla diğer atomların katsayıları yazılır.
- Asidik ve bazik ortamda yük eşitliği de sağlanmalı-dır. Asidik ortamda (+) yükün eksik olduğu tarafa H+ iyonu eklenir. Bazik ortamda (–) yükün eksik olduğu tarafa OH–iyonu eklenir. Oksijen ve hidrojen sayıla-rını eşitlemek için H O yazılır.
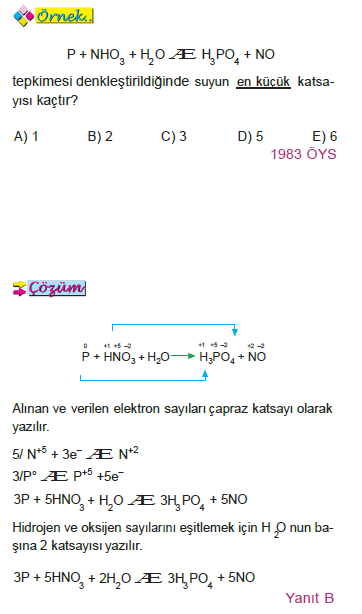
2. Yarı Tepkime Yöntemi
- İndirgenme ve yükseltgenme tepkimeleri ayrı ayrı yazılır. Değerliği değişen atomlar sayıca eşitlenir.
- Yarı tepkimelerde oksijen eşitliği sağlanır. Eşitliği sağlamak amacıyla H2O ilave edilir.
- Hidrojen eşitliğini sağlamak amacıyla asidik ortam- da H+, bazik ortamda OH– ilave edilir.
- Yük denkliğini sağlamak amacıyla gerekli tarafa elektron eklenir.
- Elektronları eşitlemek için denklemler uygun sayılar- la çarpılır ve yarı tepkimeler taraf tarafa toplanır.
Aktiflik
- Aktiflik, bir atom veya iyonun elektron alma ya da elektron verme eğiliminin bir ölçüsüdür.
- Metaller için aktiflik elektron verme eğilimi, ametaller için aktiflik elektron alma eğilimidir.
- Metallerde yükseltgenme eğilimi fazla olan daha aktiftir.
- Ametallerde indirgenme eğilimi fazla olan daha akiftir.
[ad1]
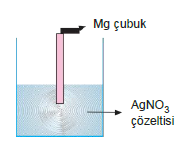
Şekilde görüldüğü gibi AgNO3 çözeltisi bulunan bir kaba Mg çubuk batırılırsa Mg nin zamanla aşındığı (Mg elektron verir ve yükseltgenir) Mg çubuk üzerinde Ag biriktiği (Ag elektron alır ve indirgenir) görülür. Burada Mg nin Ag den daha aktif olduğu söylenebilir. Mg nin yükseltgenme eğilimi Ag den fazladır


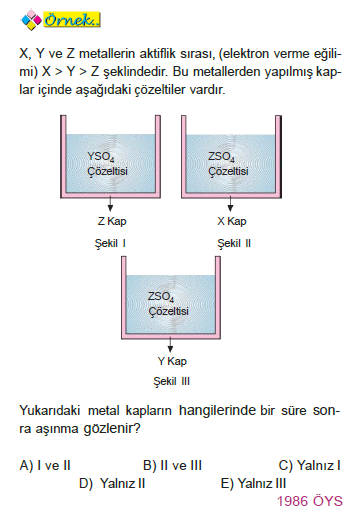
[m2]

[kimya_ygs_lys]
