Sigma (d) ve Pi (π) bağları:
İki orbitalin bağ eksenleri doğrultusunda uç uca örtüşmesiyle sigma bağı oluşur. Atomlar arasındaki tekli bağların tümü veya atomlar arasında oluşan ilk kovelent bağların tümü sigma bağlarıdır.
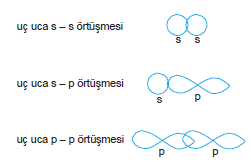
Orbital eksenlerinin paralel olarak yan yana örtüşmesiyle pi bağları oluşur.
Pi bağları sigma bağlarına göre, daha zayıftır. Tepkimelerde önce pi bağı kopar.

İki atom arasında yalnız bir tane sigma bağı oluşabilir. Sigma bağı oluşmadan pi bağı oluşmaz.
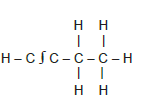
[ad1]
Molekülünde tekli bağların tümü sigma, C ∫ C bağlarının 1e sigma 2 si pi bağıdır. Molekül toplam 9 tane sigma 2 tane pi bağı içerir.

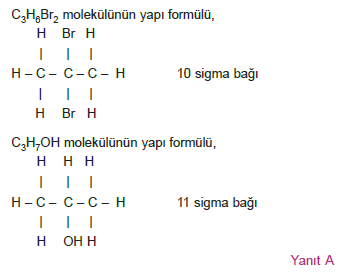
Orbital Yapısı
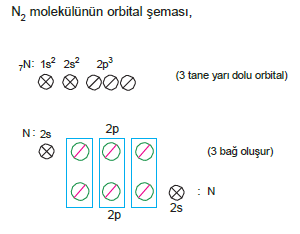
H2 molekülünün orbital şeması
1H = 1s1 (1 tane yarı dolu orbital)

[m2]
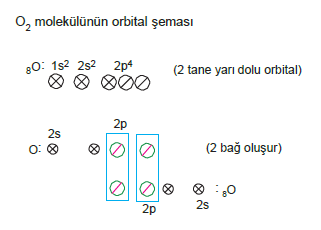
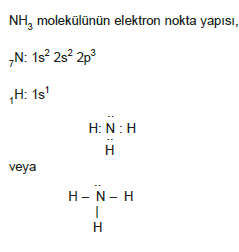
Yüksek atomlu moleküllerde elektron nokta yapısı:
- Moleküldeki atomların değerlik elektronları bulunur ve yapacakları bağ sayısı belirlenir.
- Çok bağ yapan, merkez atom olarak alınır. Diğer atomlar merkez atomun çevresine yerleştirilir.
- Birden fazla merkez atom varsa ilk olarak bu atom- lar birbirine bağlanır.
- Değerlik elektronları atomların çevresine oktet ve dublet kuralına göre yerleştirilir.


[kimya_ygs_lys]
